
不育症とは
2回以上の流産や死産の経験が
ある場合を不育症と呼びます。
流産を経験すると、言葉にできないほどのショック、深い悲しみや無力感を感じてしまうことも少なくありません。しかし実は、普通の妊娠でもその10~15%は流産になってしまい、妊娠したことのある女性のおよそ4割は流産を経験するというデータがあります。女性にとって流産を経験することは珍しいことではないのです。
その中でも2回以上の流産や死産の経験がある場合を不育症と呼びます。

流産と不育症
妊娠初期の流産の大部分60~80%は、受精のときに偶然生じた胎児の染色体異常が原因となって起こります。そして、流産の頻度や染色体異常による流産の割合は、年齢が進むにつれて高くなります。2回以上の流産や死産の経験があれば不育症といいます。すでに子供がいる場合でも、2回以上の流産や死産の経験があれば不育症に含まれます。流産や死産は、連続していなくてもよいです。特に、3回以上の流産の経験があれば習慣流産とよびますが、これも不育症の中に含まれます。日本では2回以上の流産既住の頻度は5%と報告されており、不育症女性は少なくとも34~49万人程度いると推定されています。
*3 不育症管理に関する提言2025

不育症のリスク因子と検査
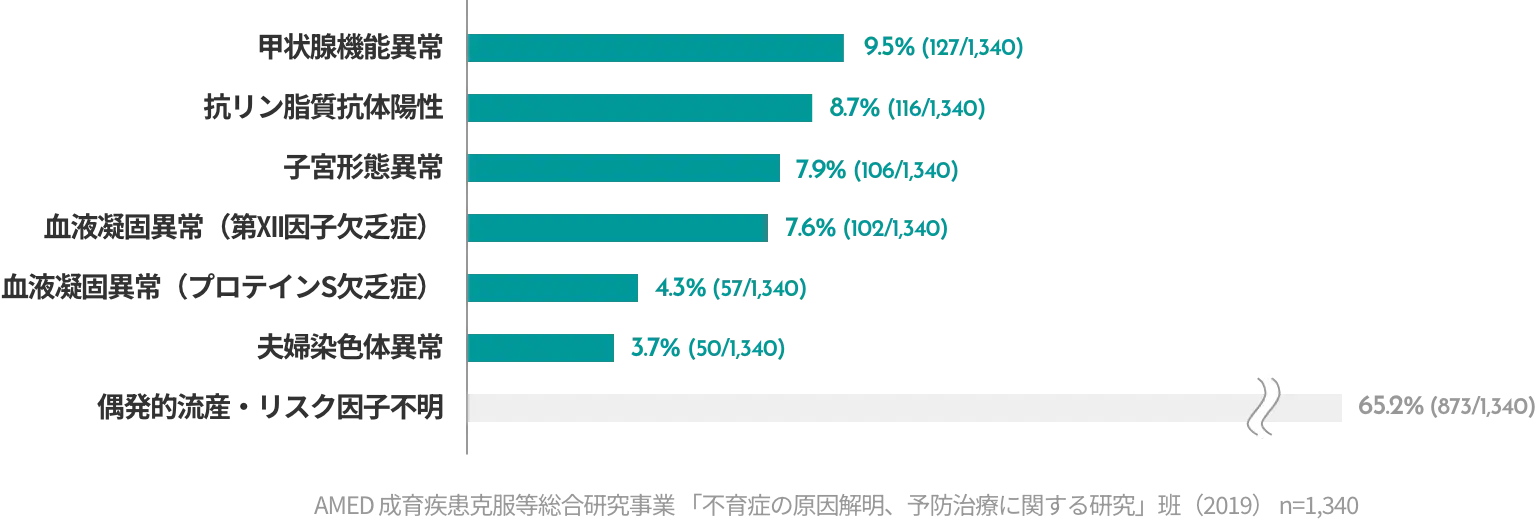
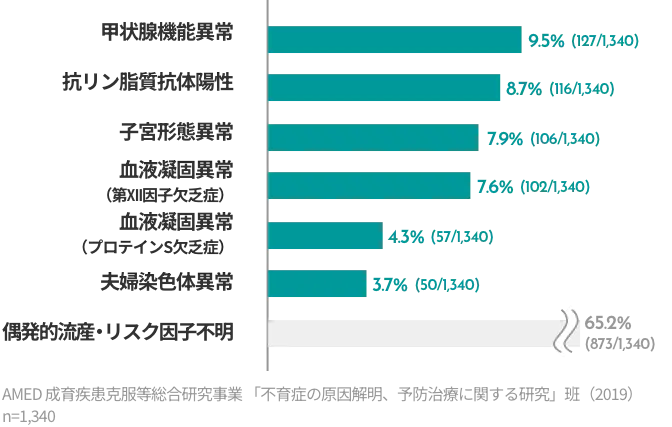
不育症を引き起こすリスクが高まる状態(リスク因子)や原因はたくさんあります。患者さんカップルそれぞれでリスク因子や原因は異なりますので、それらを特定するためには適切な検査が必要になります。検査を行うことによってリスク因子や原因が明らかになれば、最適な治療や対処ができるようになります。
-
抗リン脂質抗体陽性(8.7%)
自己抗体である抗リン脂質抗体により、血栓症や流死産を引き起こす病気です。抗リン脂質抗体症候群の分類基準(札幌基準シドニー改定 2006年)において、臨床基準(a:妊娠10週以降で他に原因のない正常形態胎児の1回以上の胎内死亡、b:重症妊娠高血圧腎症、子癇または胎盤機能不全による妊娠34週以前の形態学的異常のない胎児の1回以上の早産、c:妊娠10週以前の3回以上連続した他に原因のない習慣流産)の1項目以上、かつ検査基準のうち1項目以上が12週間以上の間隔をあけて2回以上陽性であるとき、抗リン脂質抗体症候群と診断されます。
検査項目
- 抗β2GPI抗体 IgG,IgM
- 抗カルジオリピン抗体 IgG,IgM
- β2GPI依存性抗カルジオリピン抗体
- ループスアンチコアグラント
- β2GPIネオセルフ抗体
- 抗PE抗体 IgG、IgM
- 抗PS/PT抗体
-
血液凝固異常(第Ⅻ因子欠乏症、プロテインS欠乏症)(7.6%/4.3%)
血液が固まりやすい素因(血栓性素因)は、血栓症のみならず、流産、死産および妊娠合併症のリスク因子になるとされます。
検査項目
- プロテインS
- 凝固第Ⅻ因子
- プロテインC
- アンチトロンビン
-
甲状腺機能異常(9.5%)
甲状腺機能亢進症や低下症では、流産、早産および妊娠合併症のリスクが高くなります。
検査項目
- TSH
- fT4
- 抗TPO抗体
-
子宮形態異常(7.9%)
中隔子宮(子宮の内部が壁によって左右に分かれている状態)では流産リスクが高いとされ、子宮鏡による手術が検討されます。
検査項目
- 3D超音波検査
- ソノヒステログラフィー(2D超音波検査)
- 子宮卵管造影(HSG)
- MRI
- 子宮鏡
-
夫婦染色体異常(3.7%)
夫婦のどちらかに転座等の染色体構造異常があると、流産を繰り返す原因になります。
検査項目
- 染色体G分染法
-
偶発的流産・リスク因子不明(65.2%)
妊娠年齢が高くなると、偶発的な胎児染色体異常による流産の割合が増えます。 これまでの検査法では検出できない未知のリスク因子・原因を持っている場合があり、新しい検査法の開発が進められています。
検査項目
- 流死産胎児絨毛染色体検査(G分染法)
不育症を引き起こす原因は
様々ですが、
適切な検査で
調べることができます。
不育症の治療(リスク因子別)
-
抗リン脂質抗体症候群、血液凝固異常
妊娠すると分娩時の出血に備えて血液が固まりやすくなるため、血栓症のリスクが6倍高くなると言われています。特に胎盤は血栓ができやすく、赤ちゃんに酸素や栄養が運ばれなくなり、流産や死産にいたることもあります。抗リン脂質抗体は胎盤に炎症を発生させて、流産や死産を引き起こすこともあります。抗リン脂質抗体症候群の妊娠では、低用量アスピリンや低用量アスピリン・ヘパリン併用療法によって血栓を予防し炎症を抑制することで、およそ8割が無事に出産できると言われています。アスピリンは少量(81~100mg)であることがポイントで、大量に服用すると、かえって血液をサラサラにする効果が薄れてしまいます。検査としては、β2GPI依存性抗カルジオリピン抗体、抗β2GPI抗体 IgG、IgM、抗カルジオリピン抗体IgG、IgM、ループスアンチコアグラントが保険適用となっています。臨床基準の1項目以上、かつ検査基準のうち1項目以上が12週間おいて2回以上陽性であるとき、抗リン脂質抗体症候群と診断されます。そのほかの血液凝固異常(第Ⅻ因子欠乏症やプロテインS欠乏症等)については、これまでの流産・死産歴によって低用量アスピリン単独療法やヘパリン併用療法を行うケースなどさまざまです。主治医と相談して、個別に治療法を決めて下さい。
治療法
- 低用量アスピリン療法
- 低用量アスピリン・ヘパリン併用療法
-
甲状腺機能異常
甲状腺機能異常は、20~40代の女性に多く見られ、約20人に1人は病気があると言われています。
バセドウ病などの甲状腺機能亢進症は、不育症のみならず、赤ちゃんの先天異常、早産、妊娠高血圧症候群のリスク因子になることが知られています。また、橋本病などの甲状腺機能低下症では、不妊症、流産、早産のリスクが高くなります。甲状腺機能低下症と流産とは明確な関連があります。異常が見つかった場合は、内科専門医による診断と治療を行い、甲状腺機能が正常になってから妊娠することが推奨されます。妊娠中と産後は、甲状腺機能の変動が見られるため定期的なフォローが必要です。検査としてTSHやfT4を測定し、異常があれば抗TPO抗体を測定します。ヨーロッパ生殖医学会(ESHRE)の不育症ガイドライン(2022)では、TSHと抗TPO抗体の検査を推奨していますが、日本では、はじめから抗TPO抗体の測定を行うのは一般的ではありません。まずTHSとfT4を測定し、異常がある場合に抗TPO抗体の測定を行うことが推奨されます。治療法
- 甲状腺剤、抗甲状腺剤
-
子宮形態異常
先天性の子宮形態異常があっても、母体の健康に直接影響することはほとんどなく、多くは治療の必要はありませんが、子宮は胎児が発育する場であるため、妊娠経過に影響する可能性はあります。子宮形態異常にはいろいろなタイプがあり、例えば重複子宮では流産率は高くはないとされています。中隔子宮については、子宮鏡の手術により中隔部分を切除すると出産率が高まる可能性があるとして、治療法の一つの選択肢として提示されます。しかし、手術後に妊娠率が低下したケースも報告されています。中隔子宮で軽症の場合は、手術を行わなくても無事に出産できる可能性はありますので、手術の実施についてはメリット・デメリットを考慮して、主治医と相談して方針を決めてください。子宮形態検査は、3D超音波検査が感度・特異度がともに高く、一番に推奨されます。次に推奨されるのはソノヒステログラフィー(2D超音波検査)であり、子宮卵管造影検査(HSG)はヨードや放射線被曝の影響があります。また、ソノヒステログラフィーや子宮卵管造影検査などの1次検査で子宮形態異常が疑われた時や、3D超音波検査が利用できない環境ではMRI検査を行います。先天性子宮形態異常や粘膜下筋腫を疑う場合には、子宮鏡検査を行うことがあります。
治療法
- 手術もしくは経過観察
-
夫婦染色体異常
私たちは通常23対、計46本の染色体を持っています。 時に染色体の一部が入れ替わり、他の染色体と結合する染色体構造異常が起きます。これを染色体転座といいます。転座があっても、染色体には過不足はなく、染色体全体の総量はほとんど変わらないため、本人の健康状態に影響はありません。しかし、精子や卵子ができる過程で、遺伝情報が不均衡になる可能性があり、妊娠するときに問題が生じます。妊娠初期の流産の過半数は、胎児に偶発的に起きた染色体異常によります。しかし、流産を繰り返す不育症の場合、夫婦のどちらかに染色体異常がある可能性が高くなります。不育症カップルの3~6%に染色体の総量には過不足のない均衡型の相互転座やロバートソン転座が見られます。夫婦の染色体異常の検査を受ける場合、個人情報である遺伝情報の保護、検査の意義、起こりうる問題点などについて事前に説明を受けます。
治療法
夫婦どちらかの染色体異常が不育症の原因があることを特定することで、夫婦間に不和が生じる可能性があります。どちらに原因があるかを特定せずに、結果を聞くという選択肢もありますので、事前によく話し合いをしましょう。染色体異常が発見された場合は、遺伝カウンセリングを受け、出産の確率や赤ちゃんへの遺伝の可能性等を理解したうえで、今後の方針を決めるようにしましょう。流産率は高まりますが、最終的に子どもを持てる確率は低くはありません。流産や不育症の原因と考えられる染色体異常が見つかった場合、着床前診断(PGT-A、PGT-SR)という選択肢があります。これにより流産率が低下することがわかっていますが、現在のところ子どもを持てる確率が高くなるという根拠はないため、メリット・デメリットについて理解したうえで判断しましょう。着床前診断とは、体外受精によって得られた胚の細胞の一部を採取して、染色体の数や構造を調べる検査です。体外受精や胚移植をしてもなかなか妊娠できない、妊娠しても流産してしまうケースにおいて、胚の染色体異常が原因であることがあります。着床前診断は、子宮に移植する前の段階で胚を調べることで、流産率が低い胚を選択するための検査です。欧米など諸外国では、以前からPGT-Aが行われていました。一方、日本では、「命の選別につながる」との倫理的配慮から、日本産科婦人科学会が実施を認めていませんでした。しかし、国内の実施を求める声の高まりに伴って、2017年からパイロット試験が実施され、2020年に臨床研究がスタートしました。そして2022年から、日本産科婦人科学会「着床前診断に関する見解/細則(2022年1月9日改定)」に基づき、認定された200以上の施設で一般診療として着床前診断が行われています。
PGT-A(着床前胚染色体異数性検査)
体外受精によって得られた受精卵に、偶発的に起きた染色体の数の異常を検査します。
対象者
- 体外受精・胚移植を2回以上行っても着床しなかった不妊症の夫婦
- 流産の経験が2回以上ある不育症の夫婦
PGT-SR(着床前胚染色体構造異常検査)
夫婦の染色体に、転座など何らかの構造異常がある場合に行う検査です。染色体の数だけではなく、構造異常に由来する染色体の部分的な過不足がないかを調べます。
対象者
- 夫婦いずれかに染色体構造異常が確認されている不育症(もしくは不妊症) の夫婦
-
偶発的流産・リスク因子不明
不育症の検査を一通り行っても原因やリスク因子が特定できない場合、偶発的な胎児の染色体異常による流産を繰り返した可能性があります。検査として、流死産胎児絨毛染色体検査(G分染法)があります。この検査は、流産の絨毛(胎盤の組織の一部)を取り出して染色体検査を行い、流産の原因が胎児染色体異常かどうかを調べる検査です。次の妊娠に向けた治療方針を決める上でも重要な検査です。一方で、現在の標準的な検査法では検出されない原因やリスク因子を持つ場合もあります。最新の検査法によって治療方法が見つかる可能性もありますので、個別に主治医と相談して検査と治療法を選択してください。原因不明の重症の不育症に免疫グロブリン大量療法が有効であるという報告が2022年に発表されました。妊娠時にはテンダーラビングケアによって、流産に対する不安を和らげることも重要です。
※保険適用されている流死産胎児絨毛染色体検査(G分染法)は、流産歴があり、流産手術をしたときに保険適用になります。自然排出された場合に検査可能な次世代シーケンサーを用いた検査法は、保険適用外(先進医療A)です。流死産胎児染色体検査でわかること
- 胎児の染色体に数的異常がある場合今回の治療が無効だったために流産したわけではないので、同じ治療方針で次回の妊娠に進んで問題ないと考えられます。
- 胎児の染色体に数的異常がない場合流産の原因が母体側にある可能性があり、原因やリスク因子の精査が必要です。治療法を変更する必要があるかもしれません。
- 胎児の染色体に構造的な異常がある場合夫婦染色体検査を検討する必要があります。両親のいずれかに転座など染色体の 構造異常があった場合にはPGT-SRの適応となります。
監修医のコメント
日本には多くの不育症の患者さんがおります。不育症の患者さんの悩みは計り知れないほど大きいです。次は必ず成功したい。手術をもう経験したくない。自分の体のせいかも。でも、病院に行ってもうまくいかないかもしれない。不安のため妊娠をあきらめてしまうこともあります。
すべてがうまくいくわけではありませんが、専門医の診察によって出産率が20~30%上がると言われています。不育症の医療は日進月歩です。たえず新たな検査法や治療法が編み出されていますので、次に可能性があります。このページに書かれてあります内容を参考にされて、希望をもたれて専門医の診療をぜひ受けてみてください。
医療法人渓仁会 手稲渓仁会病院 不育症センター センター長
山田秀人

Β2GPIネオセルフ抗体検査は、
不育症の検査として先進医療Aに
認定されました。
(2025年6月1日告示)

